Estudio muestra que la primera terapia intrauterina de células madre es segura para la reparación de espina bífida
UC Davis Health realizó con seguridad el primer tratamiento de espina bífida combinando cirugía fetal con células madre. Así lo demuestran los resultados de la Fase 1 de un ensayo clínico en curso. Estos resultados fueron publicados en The Lancet.
El estudio se denomina “Viabilidad y Seguridad de la Terapia Celular Intrauterina para la Reparación de Mielomeningocele (Ensayo CuRe): Primer estudio de un solo brazo, en humanos, Fase 1". Este examinó si agregar una capa de células madre placentarias a una cirugía fetal estándar podía realizarse con seguridad. La espina bífida, también conocida como mielomeningocele, ocurre cuando el tejido espinal no logra fusionarse correctamente durante las primeras etapas del embarazo. Este defecto congénito puede llevar a una serie de discapacidades cognitivas, urinarias, intestinales y de movilidad durante toda la vida.
“Poner células madre en un feto en crecimiento era totalmente desconocido. Nos alegra reportar gran seguridad”, dijo Diana Farmer, investigadora principal del Ensayo CuRe y jefa del Departamento de Cirugía de UC Davis. “Esto nos allana el camino para nuevas opciones de tratamiento para niños con defectos congénitos. El futuro es prometedor para terapias genéticas y celulares antes del nacimiento”.
La primera fase del ensayo fue financiada por una subvención de $9 millones de la agencia de células madre del estado, Instituto de Medicina Regenerativa de California (CIRM).
Sobre el tratamiento
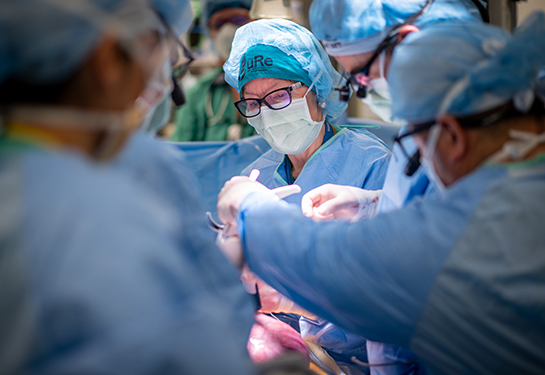
Durante la cirugía fetal, se hace una apertura pequeña en el útero. Los cirujanos luego llevan el feto hasta el punto de la incisión para poder exponer la parte de atrás del feto y el defecto de espina bífida. El equipo médico pone un parche pequeño conteniendo células madre vivas directamente sobre la médula espinal expuesta del feto, antes de cerrar las capas de la espalda para permitir que el tejido se regenere. Las células madre, obtenidas de placentas donadas, están diseñadas para proteger la médula espinal en desarrollo y evitar que sea dañada antes del nacimiento.
Es la primera terapia en el mundo de células madre en el útero para la espina bífida, y el único ensayo diseñado para mejorar los resultados de sólo la cirugía fetal en los niños.
Descubrimientos clave de la Fase 1
Los primeros tres bebés en el ensayo fueron monitoreados de cerca desde la cirugía hasta el nacimiento. Los científicos reportaron lo siguiente:
- Ninguna preocupación sobre seguridad relacionada a las células madre.
- No hubo ninguna infección, pérdida de líquidos o crecimiento anormal de tejido, y no se formó ningún tumor en el sitio de la reparación.
- Todas las cirugías tuvieron éxito, y el parche de células madre fue colocado como se había planeado en cada paciente, y todas las heridas se curaron completamente.
- Los MRIs mostraron un cambio de la hernia del cerebro posterior en todos los bebés, lo cual es un indicador del éxito de la cirugía.
- Ningún bebé requirió un tubo por hidrocefalia antes de ser dados de alta.
Porque los primeros resultados sobre seguridad fueron importantes, la Administración de Alimentos y Medicamentos (FDA por sus siglas en inglés) y una junta independiente de monitoreo aprobaron la realización de la próxima fase del estudio.
Por qué esto es importante
La espina bífida afecta entre 1,500 y 2,000 niños en Estados Unidos cada año. Si bien la cirugía fetal ha mejorado mucho desde que se introdujo hace más de una década, muchos niños tienen dificultades de movilidad y otras complicaciones de largo plazo. El Ensayo CuRe está explorando si las células madre pueden agregar poder regenerativo a la cirugía, potencialmente mejorando la movilidad y calidad de vida.

“Este es un importante paso adelante hacia una nueva forma de terapia fetal, una que no sólo repara, sino que potencialmente ayuda a curar y proteger el desarrollo de la médula espinal”, dijo Aijun Wang, coinventor de la tecnología del tratamiento de células madre placentarias e investigador co-principal del ensayo con Farmer. Es codirector del Centro de Bioingeniería Quirúrgica de UC Davis.
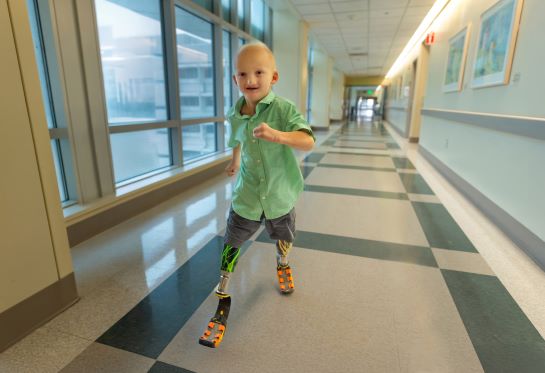
Para Michelle Johnson, participante del Ensayo CuRe, la decisión de participar en el estudio le cambió la vida.
"Nuestra familia no podría sentirse más bendecida y afortunada de participar en el Ensayo CuRe”, dijo Johnson. “Las capacidades físicas y mentales de Tobi son un milagro. Estamos eternamente agradecidos por los muchos profesionales de salud que apoyaron a Tobi en su proceso y siguen viéndolo conquistar el mundo”.
Próximos pasos
El Ensayo CuRe ahora está inscribiendo hasta 35 pacientes en la Fase 1/2a del estudio. Los niños recibirán seguimiento hasta los 6 años para evaluar la seguridad a largo plazo y también los signos tempranos de mejoramiento en las funciones vesical, intestinal y de movimiento.
La fase 1/2a del estudio es financiada por CIRM y Shriners Children’s.